새로운 간행물
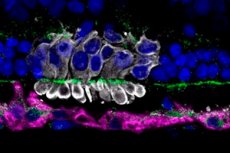
라가비 수다르산(Raghavi Sudharsan)이 이끄는 펜실베이니아 대학교 과학자들은 유도만능줄기세포(iPSC)에서 추출한 광감각 전구세포(PRPC)를 망막에 이식한 후 약 70%가 며칠 이내에 사멸하는 이유를 밝혀냈습니다. 줄기세포 연구 및 치료(Stem Cell Research & Therapy) 에 게재된 이 연구는 공여 세포의 대사 스트레스가 이러한 조기 사멸의 주범임을 시사합니다.
필수 조건
PRPC 이식은 진행성 망막 퇴행성 질환(색소망막염, 황반변성)에 유망한 치료법으로 여겨집니다. 그러나 기증 세포의 낮은 생존율은 치료 효과를 제한합니다. 지금까지는 면역 반응을 억제하는 데 중점을 두었지만, 광범위한 면역 억제에도 불구하고 손실은 여전히 심각합니다.
설계 및 방법
모델:
건강한 개와 색소성 망막염 모델 개에게 형광으로 표시된 PRPC의 망막하 주사를 맞았습니다.
생존 추정치:
플루오레세인 안지오그래피와 광간섭단층촬영(OCT)을 통해 1일차, 3일차, 7일차에 이식된 세포의 양을 기록했습니다.
단일 세포 전사체학(scRNA-seq):
PRPC는 3일째에 망막 부위에서 분리되었고, 대사 및 세포사멸과 관련된 유전자의 발현이 분석되었습니다.
면역조직화학:
이식 부위에서 산화 스트레스 마커(4-HNE), 미토콘드리아 상태(Tom20), 미세아교세포 활성화(Iba1)를 평가했습니다.
주요 결과
- 대량 세포 손실: 면역 억제에도 불구하고 건강한 망막과 퇴행성 망막 모두에서 PRPC의 약 70%가 7일차에 사라졌습니다.
- 대사 스트레스: scRNA-seq를 통해 산화적 인산화 유전자(CYCS, COX4I1)의 발현이 극적으로 감소하고 세포사멸 마커(BAX, CASP3)의 전사가 증가하는 것으로 나타났습니다.
- 미토콘드리아 기능 장애: 면역조직화학염색 결과 이식된 PRPC에서 Tom20 표지의 단편화와 손실이 나타났으며, 4-HNE 수치의 증가는 산화적 손상을 나타냈습니다.
- 미세아교세포의 역할: 이식 부위에서 Iba1⁺ 미세아교세포 활동은 PRPC 사망에 따라 증가했으며, 이는 국소 염증을 악화시키고 추가 손실로 이어질 수 있습니다.
세포 치료에 대한 의미
이러한 결과는 패러다임을 변화시킵니다. PRPC의 생착을 증가시키려면 면역 반응을 억제하는 것뿐만 아니라 공여 세포의 에너지 대사를 지원하는 것도 필요합니다. 가능한 개입 방법은 다음과 같습니다.
- 미토콘드리아 회복력을 강화하기 위해 아스트레스 부하의 경계에서 정상적인 배양 조건 하에 PRPC에 대한 예비적인 "대사 사전 훈련"을 실시합니다.
- 이식 중 및 이식 직후에 미토콘드리아 안정제(코엔자임 Q₁₀, 카르니틴) 칵테일을 사용합니다.
- 국소 망막 미세환경의 조절: 이식 부위에 항산화제나 미토콘드리아 보호제를 전달합니다.
실제적 결론과 전망
- 대사 전처리: 이식 전 경미한 대사 스트레스 조건에서 PRPC를 조절하여 회복력을 강화합니다.
- 스캐폴드 전달: 생분해성 매트릭스를 사용하여 기증 세포가 풍부한 배양 배지에서 망막 환경으로 점진적으로 전환되도록 보장합니다.
- 영양 지원: PRPC와 함께 항산화제나 미토콘드리아 호흡 기질을 제공합니다.
라가비 수다르산은 "우리는 오랫동안 면역 장벽과만 싸워왔지만, 대사 쇼크 문제를 해결하지 않으면 이식은 조기 사망에 이를 수밖에 없다는 것이 이제 분명해졌습니다."라고 결론지었습니다.
국립안과연구소의 지원을 받은 이 연구는 퇴행성 망막 질환 환자의 시력을 회복하기 위한 더욱 실행 가능한 세포 치료법의 길을 열어줍니다.

