새로운 간행물
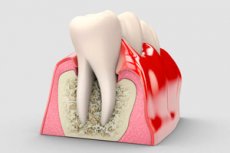
도쿄 의과치과대학(TMDU)의 연구자들은 시간 경과에 따른 치주염의 발생을 자세히 분석할 수 있는 기술을 개발했습니다.
치주염 이라고도 하는 치주 질환은 치아 상실의 주요 원인이며, 전 세계 성인 5명 중 거의 1명에게 영향을 미칩니다. 대부분의 경우, 이 질환은 치아 주변 조직의 세균 감염에 대한 염증 반응으로 발생합니다.
상태가 악화됨에 따라 잇몸이 퇴축되기 시작하여 치아와 뼈의 뿌리가 노출됩니다. 특히, 치주염 발생률은 나이가 들면서 증가하고 있으며, 전 세계 인구의 수명이 증가함에 따라 치주염의 근본 원인과 진행 과정을 확실히 이해하는 것이 중요합니다.
Nature Communications 저널 에 게재된 연구에서 TMDU의 연구진은 치주염 연구에 널리 사용되는 동물 모델을 개선하여 이 목표를 달성하는 방법을 발견했습니다.
인간의 치주염을 직접 연구하는 것은 어렵습니다. 따라서 과학자들은 종종 전임상 연구를 위해 동물 모델을 활용합니다. 예를 들어, "결찰 유도 치주염 마우스 모델"은 2012년 처음 소개된 이후 연구자들이 이 질환의 세포 기전을 연구할 수 있도록 해 왔습니다.
간단히 말해, 이 모델은 생쥐의 어금니에 실크 실을 씌워 치태를 축적시킴으로써 인위적으로 치주 질환을 유발합니다. 이 방법은 편리하고 효과적이지만, 치주염의 전체적인 양상을 포착하지는 못합니다.

치주염 발생 시 염증 유전자 발현 양상과 급성 염증에 대한 IL-33/ST2 축의 역할을 나타낸 모식도. 출처: 도쿄 의과치과대학.
"치주 조직은 치은, 치주 인대, 치조골, 그리고 백악질로 구성되어 있지만, 기술적, 양적 한계로 인해 일반적으로 치은 샘플에 대해서만 분석이 수행됩니다."라고 연구 책임자인 안하오 류(Anhao Liu)는 지적합니다. "이러한 샘플링 전략은 연구에서 도출할 수 있는 결론을 제한하기 때문에 모든 조직 구성 요소를 동시에 분석할 수 있는 방법이 필요합니다."
이러한 한계를 해결하기 위해 연구팀은 변형된 결찰 유도 치주염 모델을 개발했습니다. 기존의 단일 결찰 대신, 수컷 생쥐의 상악 좌측 어금니에 삼중 결찰을 사용했습니다. 이 전략은 제2대구치 주변 뼈를 크게 손상시키지 않으면서도 골 손실 면적을 확대하여 다양한 유형의 치주 조직을 증가시켰습니다.
"저희는 세 가지 주요 조직 유형을 분리하고 두 모델 간의 RNA 수율을 평가했습니다. 그 결과, 삼중 결찰 모델이 수율을 효과적으로 증가시켜 정상 치근 주위 조직의 양을 4배 증가시켰고, 다양한 조직 유형에 대한 고해상도 분석을 뒷받침했습니다."라고 수석 저자인 미키히토 하야시 박사는 설명했습니다.
연구진은 수정된 모델의 효과를 확인한 후, 시간이 지남에 따라 다양한 조직 유형의 유전자 발현에 대한 치주염의 영향을 연구하기 시작했으며, 특히 염증과 파골세포 분화와 관련된 유전자에 초점을 맞췄습니다.
그들의 주요 발견 중 하나는 결찰 5일 후 치근 주위 조직에서 Il1rl1 유전자의 발현이 유의미하게 증가한다는 것이었습니다. 이 유전자는 수용체와 디코이 동형체에서 ST2 단백질을 암호화하는데, 이 단백질은 염증 및 면역 조절 과정에 관여하는 IL-33이라는 사이토카인에 결합합니다.
이 유전자의 역할에 대한 더 깊은 이해를 얻기 위해 연구팀은 Il1rl1 또는 Il33 유전자가 결핍된 유전자 변형 생쥐에 치주염을 유발했습니다. 이 생쥐들은 염증성 골 파괴가 가속화되는 양상을 보였는데, 이는 IL-33/ST2 경로의 보호적 역할을 강조합니다. ST2 단백질을 수용체 형태로 함유하는 세포(mST2)에 대한 추가 분석 결과, 이들 대부분이 대식세포에서 유래한 것으로 밝혀졌습니다.
"대식세포는 일반적으로 활성화 여부에 따라 염증 촉진 세포와 항염증 세포, 두 가지 주요 유형으로 분류됩니다. mST2 발현 세포는 두 유형의 대식세포의 일부 마커를 동시에 발현한다는 점에서 독특했습니다."라고 선임 저자인 이와타 타카노리 박사는 설명했습니다. "이 세포들은 염증이 시작되기 전에 치근단 주위 조직에 존재했기 때문에 '치주 조직 상주 대식세포'라고 명명했습니다."
종합적으로, 이 연구의 결과는 변형된 동물 모델을 이용하면 생물 분자 수준까지 더욱 세부적으로 치주염을 연구할 수 있다는 것을 보여줍니다.
"저희는 치주 질환에서 염증과 골 파괴를 조절하는 새로운 IL-33/ST2 분자 경로와 치주 질환에 깊이 관여하는 치근단 주위 조직의 특정 대식세포의 가능성을 제시합니다. 이는 새로운 치료 전략 및 예방법 개발로 이어질 수 있기를 바랍니다."라고 수석 저자인 나카시마 토모키 박사는 결론지었습니다.

