새로운 간행물
위스타 연구소의 필리포 베글리아 준교수 박사와 그의 팀은 심각하고 종종 치명적인 뇌암인 신경교 종이 면역 체계를 억제하여 종양이 신체의 방어력에 굴하지 않고 자랄 수 있는 핵심 메커니즘을 발견했습니다.
이들의 발견은 저널 Immunity 의 "포도당 주도 히스톤 락틸화는 신경교종에서 단핵구 유래 대식세포의 면역 억제 활동을 촉진한다"라는 논문에 게재되었습니다.
베글리아 박사는 "이번 연구는 암의 자가 증식 메커니즘을 충분히 이해한다면 질병에 매우 효과적으로 대처할 수 있음을 보여줍니다."라고 말했습니다.
"저는 향후 신경교종에서 대사 매개 면역 억제 메커니즘에 대한 연구를 기대하고 있으며, 이 암을 더 잘 이해하고 퇴치하는 방법에 대해 계속해서 더 많이 배울 수 있기를 바랍니다."
지금까지 단핵구 유래 대식세포와 미세아교세포가 어떻게 신경교종에서 면역억제적 종양 미세환경을 만들어내는지에 대한 연구는 거의 이루어지지 않았습니다.
Veglia 연구실은 신경교종에서 면역억제의 세포적 메커니즘을 조사하였고, 신경교종이 진행됨에 따라 단핵구 유래 대식세포가 미세아교세포보다 많아지는 것을 발견하였습니다. 이는 종양 미세환경에서 단핵구 유래 대식세포가 우세한 것이 면역 회피 측면에서 암에 유익하다는 것을 시사합니다.
실제로, 단핵구 유래 대식세포는 미세아교세포와는 달리 전임상 모델과 환자에서 T 세포(종양 세포를 죽이는 면역 세포)의 활동을 차단했습니다. 연구팀은 단핵구 유래 대식세포의 수를 인위적으로 줄인 전임상 교모세포종 모델을 평가하여 이를 확인했습니다.
예상대로, 종양 미세환경에서 악성 대식세포가 적은 모델은 표준 신경교종 모델과 비교하여 향상된 결과를 보였습니다.
교모세포종은 뇌에서 발생하는 모든 악성 종양의 절반 이상을 차지하며, 진단받은 환자의 예후는 매우 좋지 않습니다. 진단 후 1년 생존율은 25%에 불과합니다. 교모세포종은 뇌에 위치할 뿐만 아니라 면역 억제성 종양 미세환경 때문에 위험하며, 이로 인해 유망한 면역 치료법 에 내성을 보입니다.
대식세포(단핵구 유래 대식세포와 미세아교세포)와 같은 특정 면역 세포를 종양에 대항하기보다는 종양을 위해 일하도록 프로그래밍함으로써, 신경교종은 항암 면역 반응을 회피하면서 암이 공격적으로 자랄 수 있는 종양 미세환경을 스스로 만듭니다.
메커니즘의 명확화
단핵구 유래 대식세포의 역할을 확인한 후, Weglia 연구실은 이 암 관련 면역 세포가 면역 체계에 어떻게 작용하는지 정확히 이해하고자 했습니다.
그들은 대식세포의 염기서열을 분석하여 면역억제에 역할을 하는 유전자를 나타낼 수 있는 비정상적인 유전자 발현 패턴이 있는지 확인했고, 또한 대식세포의 대사 패턴을 조사하여 비정상적인 유전자 발현이 대사와 관련이 있는지 알아보았습니다.
유전자 및 대사 분석을 통해 포도당 대사가 유도되었습니다. 일련의 검사 결과, 포도당 대사가 증가하고 포도당의 주요 수송체인 GLUT1을 발현하는 단핵구 유래 대식세포가 인터루킨-10(IL-10)을 분비하여 T 세포 기능을 저해하는 것으로 나타났습니다.
연구팀은 신경교종이 이들 대식세포의 포도당 대사를 방해하여 면역 억제 활동을 유발한다는 것을 입증했습니다.
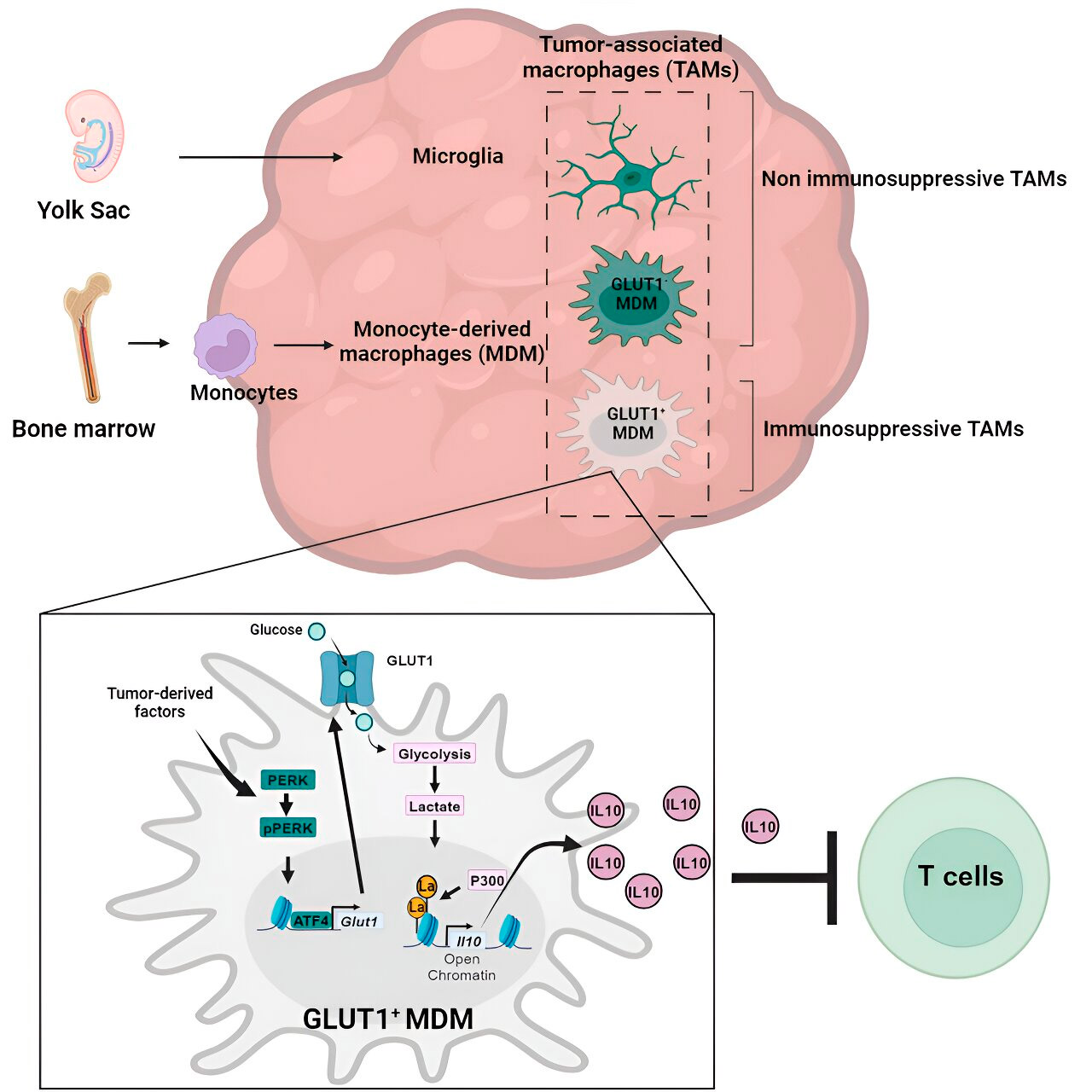
히스톤 락틸화와 그 역할
연구진은 단핵구 유래 대식세포의 포도당 대사 관련 면역 억제 활동의 핵심이 "히스톤 락틸화"라는 과정에 있다는 것을 발견했습니다. 히스톤은 유전체의 구조 단백질로, 특정 상황에서 IL-10과 같은 유전자의 발현에 핵심적인 역할을 합니다.
단핵구 유래 대식세포는 포도당을 빠르게 대사하여 포도당 대사의 부산물인 젖산을 생성합니다. 히스톤은 "락틸화"(즉, 젖산이 히스톤에 통합됨)될 수 있으며, 이러한 히스톤 구조는 단핵구 유래 대식세포가 암세포 성장을 지원하기 위해 생성하는 IL-10의 발현을 촉진합니다.
문제에 대한 해결책
그렇다면 포도당 대사와 관련된 단핵구 유래 대식세포의 면역 억제 활동을 어떻게 막을 수 있을까요? 베글리아 박사와 그의 연구팀은 가능한 해결책을 찾아냈습니다. 바로 대식세포에서 포도당 대사와 GLUT1 발현을 조절하는 효소인 PERK입니다.
신경교종의 전임상 모델에서 PERK를 표적으로 삼으면 히스톤 락틸화와 대식세포 면역 억제 활동이 손상되었고, 면역 요법과 병용했을 때는 신경교종 진행이 차단되고 장기 면역이 유도되어 뇌를 종양 재성장으로부터 보호했습니다. 이는 PERK-히스톤 락틸화 축을 표적으로 삼는 것이 이 치명적인 뇌암을 퇴치하는 실행 가능한 전략이 될 수 있음을 시사합니다.

