새로운 간행물
신경과 켄 앤 루스 데이비 신경종양학과 교수인 시위안 청 박사 연구실의 한 연구에서 신경교종 종양 세포에서 선택적 RNA 스플라이싱(alternative RNA splicing)의 새로운 기전을 규명했으며, 이는 새로운 치료 표적으로 활용될 수 있을 것으로 기대됩니다. 이 연구 결과는 Journal of Clinical Investigation 에 게재되었습니다.
"우리는 대체 스플라이싱이라는 관점에서 신경교종을 치료하는 새로운 방법을 발견했고, 이전에는 확인되지 않았지만 신경교종 악성 종양에 중요한 새로운 표적을 발견했습니다."라고 이 연구의 주저자이자 신경과 조교수인 샤오 송(Xiao Song) 박사가 말했습니다.
신경교종은 성인에서 가장 흔한 원발성 뇌종양으로, 중추신경계에 존재하며 주변 뉴런을 지지하는 신경교세포에서 유래합니다. 신경교종은 유전적 및 후성유전학적 이질성으로 인해 방사선 치료 및 항암 화학요법을 포함한 표준 치료에 매우 잘 반응하지 않으므로, 새로운 치료 표적을 찾아야 할 필요성이 대두되고 있습니다.
Cheng 연구실에서 Cancer Research 저널 에 발표한 이전 연구 에 따르면, 중요한 스플라이싱 요소인 SRSF3가 정상 뇌에 비해 신경교종에서 상당히 증가되어 있으며, SRSF3에 의해 조절되는 RNA 스플라이싱이 종양 세포에서 여러 세포 과정에 영향을 미쳐 신경교종의 성장과 진행을 촉진하는 것으로 나타났습니다.
RNA 스플라이싱은 인트론(RNA의 비코딩 영역)을 제거하고 엑손(코딩 영역)을 결합하여 세포에서 유전자 발현을 지원하는 성숙한 mRNA 분자를 형성하는 과정입니다.
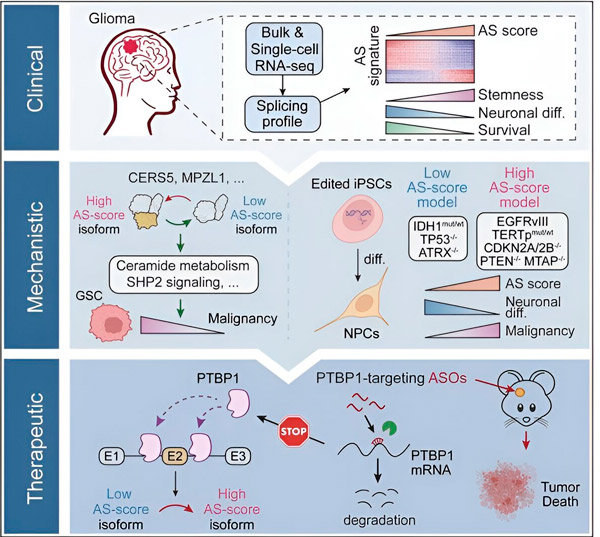
이번 연구에서 과학자들은 신경교종 종양 세포의 대체 스플라이싱 변화를 식별하고, 이러한 변화의 근본적인 메커니즘을 밝히며, 이것이 치료 표적으로서의 잠재력을 갖는지 확인하는 것을 목표로 했습니다.
연구진은 컴퓨터 기법과 RNA 시퀀싱 기술을 사용하여 환자 검체에서 채취한 신경교종 종양 세포의 스플라이싱 변화를 조사했습니다. 이러한 변화를 확인하기 위해 CRISPR 유전자 편집 기술을 사용하여 인간 유도만능줄기세포(iPSC)에서 유래한 신경교종 모델에 다양한 신경교종 유전자 돌연변이를 도입했습니다.
연구진은 이러한 스플라이싱 변화가 많은 종양(신경교종 포함)에서 과발현되는 것으로 알려진 상피 성장 인자 수용체 III(EGFRIII) 변이체에 의해 증가되고, IDH1 유전자의 돌연변이에 의해 억제된다는 것을 발견했습니다.
연구자들은 서로 다른 아미노산 서열을 갖는 서로 다른 단백질 동형체를 생성하는 두 가지 RNA 스플라이싱 사건의 기능을 확인했습니다.
"이러한 동형 단백질 중 오직 하나만이 종양 성장을 촉진할 수 있는데, 다른 동형 단백질은 정상적인 뇌에서 정상적으로 발현됩니다. 종양은 이러한 메커니즘을 이용하여 정상적인 뇌 동형 단백질보다 종양을 촉진하는 동형 단백질을 선택적으로 발현합니다."라고 송 박사는 말했습니다.
연구팀은 상류 RNA 결합 단백질을 분석하여 PTBP1 유전자가 신경교종 세포에서 종양 촉진 RNA 스플라이싱을 조절한다는 것을 발견했습니다. 면역결핍 마우스에서 동소성 신경교종 모델을 이용하여, 연구진은 안티센스 올리고뉴클레오타이드(ASO) 기반 치료법으로 PTBP1을 표적으로 삼았고, 궁극적으로 종양 성장을 억제했습니다.
연구 저자들은 "저희 데이터는 대체 RNA 스플라이싱이 신경교종의 악성도와 이질성에 영향을 미치는 역할과 성인 신경교종 치료에 있어 치료적 취약성으로서의 잠재력을 강조합니다."라고 기술했습니다.
연구진의 다음 단계는 PTBP1을 표적으로 삼아 항종양 면역 반응을 이끌어낼 수 있는 가능성을 탐구하는 것이라고 송 박사는 말했다.
"장문 RNA 시퀀싱 분석을 통해 신경교종 세포에서 PTBP1을 표적으로 삼으면 정상 조직에는 존재하지 않는 여러 개의 선택적 스플라이싱 전사체가 생성된다는 것을 발견했습니다. 따라서 저희의 다음 프로젝트는 이 동형단백질이 면역 체계가 종양을 더 잘 인식할 수 있도록 항원을 생성할 수 있는지 확인하는 것입니다."라고 송 박사는 말했습니다.
송 교수는 또한 그들의 팀이 면역 세포와 같은 신경교종 환자의 비종양 세포의 스플라이싱 변화를 분석하는 데 관심이 있다고 덧붙였다.
"우리는 스플라이싱이 세포 기능 조절에 매우 중요하다는 것을 이미 알고 있습니다. 따라서 스플라이싱은 종양 악성도를 조절할 뿐만 아니라 면역 세포의 기능도 조절하여 암을 효과적으로 사멸시킬 수 있는지 여부를 판단할 수 있습니다. 따라서 종양에 침투한 면역 세포에서 생물정보학적 분석을 수행하여 면역 세포가 종양에 침투한 후 스플라이싱에 변화가 있는지 확인하고 있습니다.
송 박사는 "우리의 목표는 면역 억제적 종양 미세환경을 형성하는 데 있어 대체 스플라이싱의 역할을 결정하고, 신경교종에서 면역 치료의 효능을 개선하기 위한 잠재적인 표적을 찾아내는 것입니다."라고 말했습니다.

